Vous souhaitez améliorer la notation des bases de données pour la métabolomique LC/MS ? Essayez les colonnes ACQUITY Premier !
Après une nouvelle erreur d'affectation, je savais qu'il devait y avoir un meilleur moyen d'améliorer ma mise en correspondance des bases de données ! La mise en correspondance des bibliothèques spectrales fait partie intégrante du flux de travail des analyses non ciblées, ou des analyses par spectrométrie de masse à haute résolution, telles que la métabolomique urinaire ou plasmatique. La comparaison d'échantillons non malades et malades peut donner un aperçu des voies biologiques potentielles qui jouent un rôle important dans la progression de la maladie. Les scientifiques sont alors en mesure de se concentrer sur ces domaines pour mettre au point de nouvelles thérapies et/ou des tests de diagnostic. Cependant, pour identifier ces métabolites, nous soumettons nos données à des recherches dans des bases de données. Il existe plusieurs bases de données commerciales que l'on peut acheter ; certaines contiennent des spectres conservés et d'autres des structures soumises à une fragmentation théorique dans un logiciel. Un facteur important dans la mise en correspondance des bibliothèques est la qualité des données de votre analyse. Un nombre trop faible ou trop élevé de pics par rapport à la référence peut avoir un impact négatif sur votre score. En cas d'attribution incorrecte, vous risquez de vous tromper de cible et de passer à côté d'un indice essentiel.
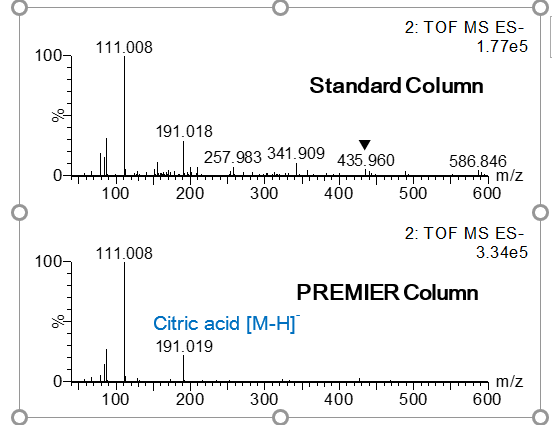
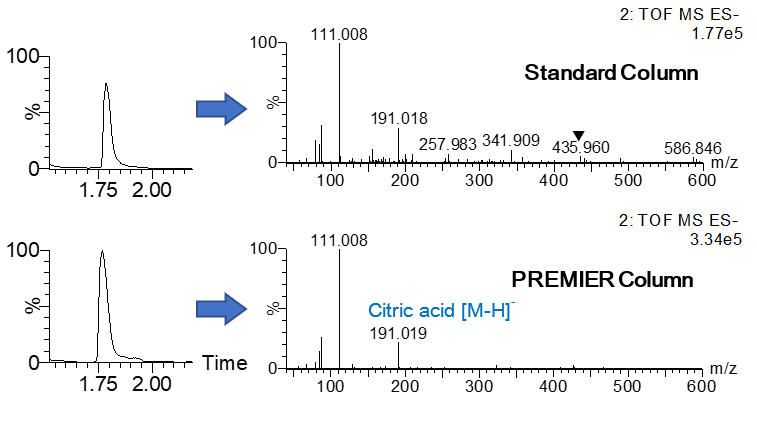
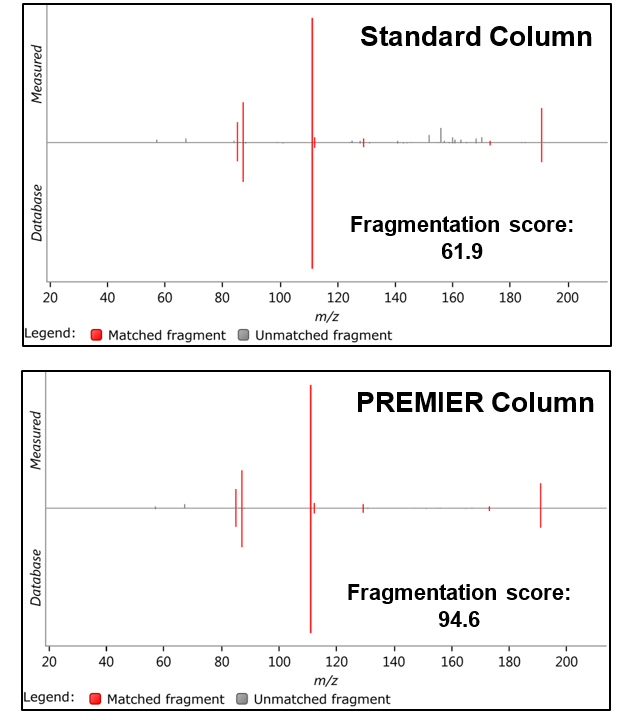
Prenons l'exemple de l'acide citrique. Il est présent dans les cellules dans le cadre du cycle de l'acide tricarboxylique (TCA). L'acide citrique est bien connu pour son interaction avec les métaux, notamment le fer. La présence de fer dans le système peut être problématique en provoquant une perte d'analyte ou des adduits dans le spectre de masse. Grâce aux colonnes ACQUITY PREMIER, nous sommes en mesure d'atténuer l'interaction de ces composés avec les métaux. La figure 1 montre les spectres à haute énergie (ou fragmentation) de l'acide citrique provenant d'un échantillon d'urine humaine diluée, analysé sur une colonne avec un matériel standard (en haut), et une colonne avec un matériel ACQUITY Premier Column (en bas). Nous voyons immédiatement la différence dans les spectres, la colonne Premier d'ACQUITY présentant un spectre plus propre et moins compliqué. Notamment, nous voyons beaucoup moins du complexe connu Fe-Citrate, 435.9 m/z [1], en utilisant la colonne Premier d'ACQUITY. Cela se traduit par des scores de fragmentation plus élevés lors de la recherche dans une bibliothèque de spectres (figure 2) et vous facilite certainement la vie au laboratoire..
Les analyses difficiles comme celles-ci font que le passage aux colonnes Premier d'ACQUITY est une évidence.
Références :
Silva A et al. Dalton Transactions. 2009(40), 8616-8625

OU :
Ressources supplémentaires :
Vidéo : Solution ACQUITY Premier avec MaxPeak High Performance Surfaces (HPS) - Comment ça marche
Blog : Le mystère de la perte d'échantillons
Blog : Besoin de soulager l'acide polaire en phase inversée
Blog : Nuits tardives au laboratoire
Blog : Où est passé mon échantillon ?
En savoir plus sur les colonnes Premier d'ACQUITY
Sujets populaires
ACQUITY QDa (16) bioanalyse (11) produits biologiques (14) biopharma (26) biopharmaceutique (36) biosimilaires (11) biothérapeutique (16) étude de cas (16) chromatographie (14) intégrité des données (21) analyse alimentaire (12) HPLC (15) LC-MS (21) chromatographie liquide (LC) (19) détection de masse (15) spectrométrie de masse (MS) (54) développement de méthodes (13) STEM (12)


