Chapitre et verset : L'USP 621 et vous

In August 2014, the United States Pharmacopeia and the National Formulary (USP-NF) put into effect new guidelines to “allowable adjustments” in its Chapter <621> (USP37-NF32 S1). And as of August 1, 2016 when USP 39 NF 34 S1 goes into effect, for <621> nothing significant has changed since.
L'USP ne publie pas ouvertement les modifications apportées à ses directives, mais ces modifications ont été annoncées sur son site Web bien avant l'entrée en vigueur des nouvelles directives.
Il ne s'agit pas de règlements, en soi. Mais, aux États-Unis du moins, la Food and Drug Administration (FDA) les traite comme des paramètres pour ses règlements.
Ainsi, comme un piéton marchant sur les voies ferrées sur la trajectoire d'un train qui arrive, il est probablement préférable de tenir compte des feux clignotants, de peur de se retrouver du mauvais côté de 10 000 tonnes d'acier en mouvement rapide.
(Alerte spoiler : le train gagne toujours .)
USP Chapter <621>, you say?
The USP-NF is a book of pharmacopeial standards that has been designated by the FDA as the official compendia for drugs marketed in the United States. Its chapter on Chromatography is <621>, found here, and “defines the terms and procedures used in chromatography and provides general information.” Specifically, it explains the allowable adjustments to chromatography systems in order to meet system suitability requirements.
Un guide des lignes directrices.
Les récents changements ont été influencés par un document de stimulation de 2009 rédigé par le Dr. Uwe Neue et al, qui proposait des applications scientifiques des méthodes de graduation. Bien que ce document ait suggéré des changements pour le transfert des méthodes isocratiques et à gradient, l'USP a mis en œuvre les changements pour les méthodes isocratiques uniquement.
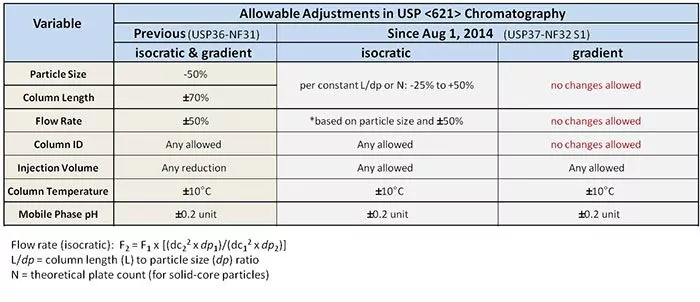
Auparavant, les changements relatifs à la taille des particules étaient autorisés, à condition qu'ils soient réduits à 50 %. La longueur des colonnes pouvait être augmentée ou diminuée de 70 %, les débits pouvaient être augmentés ou diminués de 50 %, et le diamètre interne de la colonne pouvait être modifié à volonté. Souple ? Oui. En apparence, mais une réduction de 50 % d'une taille de particule de 5 µm ne nous amène qu'à 2,5 µm, et non aux toutes nouvelles particules de moins de 2 µm.
Désormais, pour les méthodes isocratiques, les modifications de la taille des particules et de la longueur de la colonne sont traitées comme un rapport, plutôt que comme des paramètres discrets, qui peuvent diminuer de 25 % ou augmenter de 50 %, tandis que le débit peut toujours augmenter ou diminuer de 50 %. Tous les changements apportés à la D.I. de la colonne sont autorisés. En fonction de la longueur de votre colonne, les toutes nouvelles particules de moins de 2 µm peuvent maintenant être utilisées, sans validation.
Toutefois, pour les méthodes par gradient, aucune modification n'est autorisée dans les domaines suivants : taille des particules, longueur de la colonne, débit ou diamètre interne de la colonne.
Toujours avec moi ?
Voir le tableau pratique ci-dessous. Parce que, des photos.
Merci pour la photo, maintenant qu'est-ce que ça veut dire ?
En restant dans les paramètres des "ajustements autorisés" des méthodes isocratiques, les analystes peuvent simplement effectuer une vérification de la performance de la méthode et éviter les étapes de revalidation qui prennent beaucoup de temps.
Et donc...
Ainsi, les chromatographes ont désormais la possibilité de mettre en œuvre la toute dernière technologie de colonne tout en respectant les monographies existantes. Cela signifie, en bref, la possibilité d'adopter des méthodes plus avant-gardistes dans le laboratoire qui, au final, peuvent conduire à une réduction de la consommation de solvants, à des temps d'analyse plus rapides et à une augmentation globale du retour sur investissement.
Non, vous ne courrez pas à votre perte si vous n'adoptez pas l'UPLC/UHPLC.
Du moins, pas encore. Pour ceux qui utilisent des méthodes isocratiques, le chemin vers une plateforme UPLC est très clair. Selon un livre blanc publié par Waters, "la flexibilité des nouvelles directives ouvre désormais la possibilité de transférer les anciennes méthodes HPLC isocratiques vers l'UPLC sans investissement en temps et sans les tracas de la revalidation, tout en réalisant les gains d'efficacité et de productivité globaux du laboratoire grâce à des analyses à plus haut débit".
En termes plus simples, l'exploitation de la technologie des colonnes à particules de moins de 2 µm peut se traduire par un gain de temps de près de 10 fois et une diminution de plus de 15 fois de la consommation de solvants. Ajoutez à cela des outils tels que l'Empower 3 Method Validation Manager (MVM), qui vous permet d'effectuer la validation des méthodes chromatographiques - de la planification du protocole au rapport final - dans une seule application, et réduisez le temps et le coût de la validation des méthodes jusqu'à 80 %.
Je vous laisse faire le calcul. Ou économisez votre temps et laissez Waters faire le calcul pour vous.
Hélas, les méthodes de gradient sont plus populaires dans leur utilisation.
Toutefois, compte tenu des nouvelles directives, toute modification de la configuration des colonnes pour les méthodes existantes nécessite désormais une revalidation complète.
Lorsqu'une méthode ne répond pas aux exigences d'adéquation du système ? Revalidation.
Vous utilisez actuellement une méthode officinale avec des modifications qui étaient auparavant autorisées ? Elles ne le sont plus.
Du moins, pas sans revalidation.
Ce n'est pas une raison pour vous lancer dans l'aventure Office Space sur votre système HPLC et courir ensuite acheter une plateforme UPLC. (Si, pour quelque raison que ce soit , vous décidez de suivre cette voie, assurez-vous de le faire en vidéo. Vous savez, "viral").
Mais, bien que la CLHP soit toujours aussi robuste et que vous puissiez continuer à utiliser les anciennes méthodes sans avoir à changer radicalement de technologie, il peut être utile d'envisager de revalider les meilleurs outils disponibles. Si vous le faites sur une ancienne technologie, vous risquez de perdre du temps et des ressources.
S'amuser avec des acronymes - AQC et QbD.
En concevant l'UPLC il y a dix ans, Waters a permis à ses clients non seulement d'aller plus vite, mais aussi de voir plus.
Voir plus signifie être capable de mieux reconnaître les attributs critiques de qualité (CQA), afin que les analystes puissent mieux comprendre les produits. Avoir accès à de meilleures informations signifie avoir la capacité de prendre de meilleures décisions.
Tout cela est lié à une approche de la qualité par la conception (QbD) d'un produit, dans laquelle la qualité est intégrée à la fois dans le produit et dans le processus, ce qui permet d'atténuer les risques lors de la fabrication et de l'analyse du produit.
Et maintenant, après la leçon de soupe à l'alphabet, qu'est-ce que ça a à voir avec vous ?
Franchement, le train d'acier susmentionné. Sans parler de vos clients.
La FDA a publié des directives selon lesquelles les analystes devraient commencer à réfléchir davantage au cycle de vie de leurs méthodes. Par exemple, si une méthode continue à ne pas répondre aux exigences d'adéquation du système, il est peut-être temps de passer à une technologie plus récente, comme l'UHPLC ou l'UPLC, afin de mieux comprendre cette méthode.
En bref, comprenez ce qu'il y a dans la sauce, et ne vous contentez pas de suivre le livre de cuisine.
En fin de compte, les consommateurs bénéficient également du passage des laboratoires à une nouvelle technologie à haute résolution et de la possibilité d'en savoir plus sur un produit. Plusieurs affaires impliquant l'utilisation de la technologie UPLC pour découvrir des dangers précédemment inconnus dans des produits ont été fortement médiatisées au cours de la dernière décennie, notamment la mélamine dans les préparations pour nourrissons et les complications/morts liées à l'héparine.
La science ne cesse d'avancer.
Et avec elle, les règlements non plus. Ce pas de l'USP vers la modernisation des méthodes introduit un point de réflexion opportun en ce qui concerne l'utilisation du temps et des ressources précieuses pour les laboratoires et, en fin de compte, pour les entreprises soucieuses du cycle de vie de leurs technologies et du rendement des investissements technologiques qui en découle.
Ressources supplémentaires :
- Future-Proof Solutions for Regulated Laboratories In the Face of Changing USP <621> Guidelines
- Volume de puits et volume extra-colonne : Que sont-ils et comment influencent-ils le transfert de méthode ?
- Modernisation de la méthode USP en utilisant les changements autorisés "L/dp équivalent" et "N équivalent" avec les colonnes CORTECS C8 Solid-Core
Sujets populaires
ACQUITY QDa (16) bioanalyse (11) produits biologiques (14) biopharma (26) biopharmaceutique (36) biosimilaires (11) biothérapeutique (16) étude de cas (16) chromatographie (14) intégrité des données (21) analyse alimentaire (12) HPLC (15) LC-MS (21) chromatographie liquide (LC) (19) détection de masse (15) spectrométrie de masse (MS) (54) développement de méthodes (13) STEM (12)