Pruebas de cribado neonatal de segundo nivel: mejora de la especificidad de uno de los mayores logros de la salud pública

El cribado de enfermedades hereditarias en los recién nacidos ha sido anunciado como uno de los 10 mayores logros en materia de salud pública de la primera década del siglo XXI.1
La capacidad de identificar de forma presintomática a los recién nacidos con riesgo de desarrollar trastornos endocrinos, hematológicos y metabólicos ha mejorado o salvado de forma espectacular miles de vidas (y ha ahorrado millones de dólares al sistema sanitario) desde que se utilizó el primer ensayo de inhibición bacteriana del Dr. Robert Guthrie para detectar la fenilcetonuria (PKU) en los recién nacidos. Hoy en día, el impacto positivo de los programas nacionales de cribado neonatal es indiscutible.
Al igual que la prueba del Dr. Guthrie para la PKU, el objetivo principal de todas las pruebas de cribado de los recién nacidos es realizar un cribado rápido y económico de toda la población de recién nacidos atendida poco después del nacimiento. Estas pruebas son de cribado y deben tener un alto grado de sensibilidad diagnóstica para no pasar por alto a los bebés que realmente tienen un trastorno. En la búsqueda de la mayor sensibilidad posible, algunas pruebas de cribado primario de recién nacidos tienen una especificidad diagnóstica inferior a la deseable, lo que da lugar a un cierto número de falsos positivos (bebés identificados con riesgo de padecer un trastorno que finalmente no lo tienen). Se trata de una decisión consciente tomada por la comunidad de cribado neonatal, ya que el daño resultante de omitir un diagnóstico supera con creces los posibles daños asociados a la generación de una "falsa alarma".
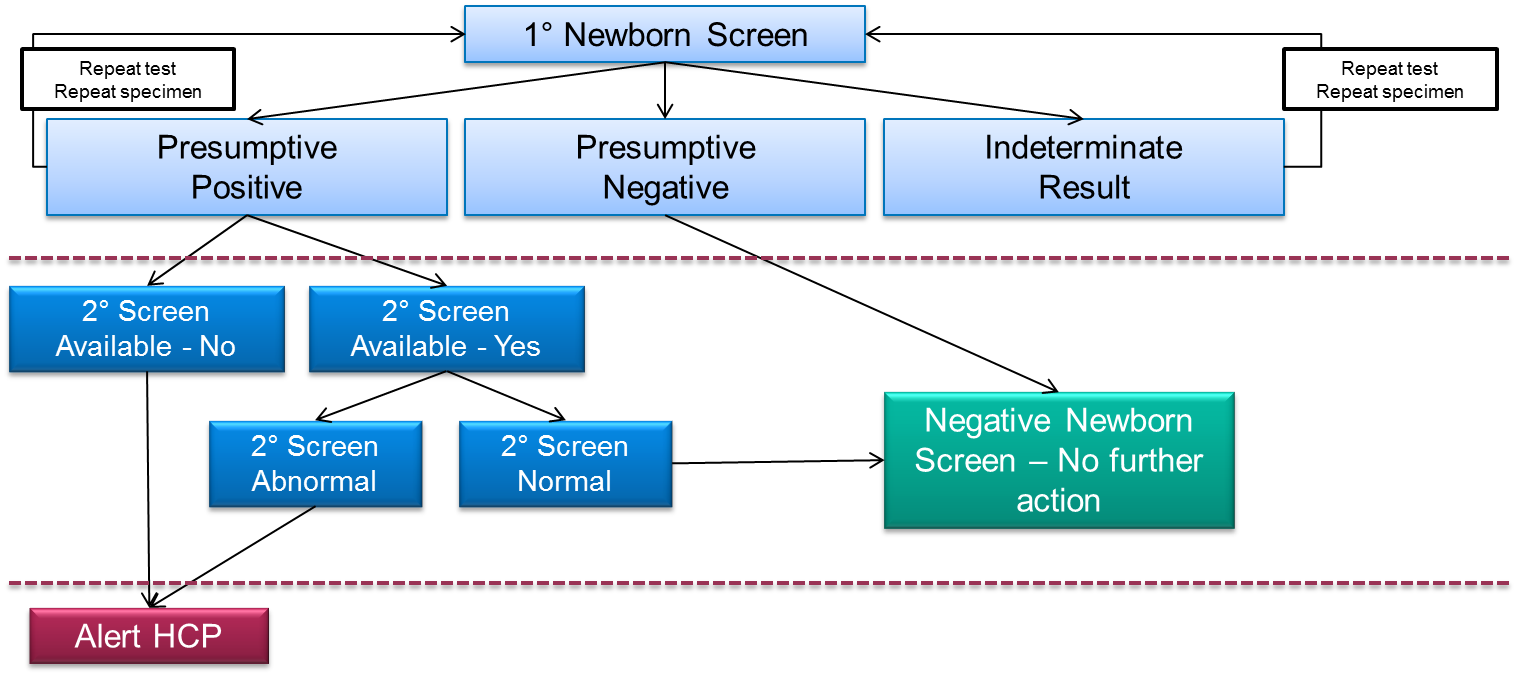
Figura 1. Ejemplo de árbol de decisión de cribado neonatal cuando se dispone de una prueba de cribado de segundo nivel. Las mismas muestras que dan un resultado positivo en la prueba de cribado primario se remiten a una prueba de cribado de segundo nivel (que suele basarse en LC-MS/MS) que tiene un mayor grado de especificidad diagnóstica. El objetivo de estas pruebas es proporcionar información adicional sobre la muestra que permita al laboratorio emitir un juicio más preciso sobre el riesgo de enfermedad, lo que debería eliminar el seguimiento innecesario de los bebés no afectados.
Independientemente de ello, los resultados falsos positivos de las pruebas causan daños como, por ejemplo, la ansiedad de los padres2 y las pruebas médicas innecesarias con su gasto concomitante. Por ello, la comunidad de cribado neonatal intenta minimizar el número de falsos positivos que produce. Una forma de hacerlo es ofrecer pruebas de cribado neonatal de segundo nivel que se aplican a todas las pruebas positivas que resultan del cribado neonatal primario (Figura 1). La prueba de cribado primaria podría ser un sistema de análisis de inyección de flujo basado en la espectrometría de masas (FIA-MS/MS), pero también podría ser un inmunoensayo u otra plataforma tecnológica. Una prueba de segundo nivel es una prueba adicional que se lleva a cabo en un nuevo disco o discos, perforados a partir de la muestra primaria de mancha de sangre seca (en otras palabras, no se toma una nueva muestra del bebé).
Muchas pruebas de cribado primario tienen un alto valor predictivo positivo, incluso sin utilizar una prueba de segundo nivel. Para estos analitos, un resultado de cribado fuera del rango de referencia del laboratorio es altamente probable que indique la presencia de la enfermedad objetivo. Sin embargo, para varios otros, un resultado positivo del cribado primario se asocia con un menor grado de confianza. En el caso de estos analitos o condiciones, existe una probabilidad razonable de que el resultado positivo de la prueba de cribado acabe por no diagnosticar la enfermedad. Las pruebas de cribado que son candidatas a la adición de una prueba de segundo nivel suelen ser las que tienen una baja especificidad diagnóstica o analítica, ya sea porque el resultado anormal se asocia con varias enfermedades o afecciones benignas no objetivo, o porque la plataforma de cribado primario es incapaz de distinguir el analito objetivo de varias interferencias.
Un ejemplo de prueba con una interferencia analítica es la detección de especies isobáricas de leucina por FIA-MS/MS. La ausencia de separación por LC de la leucina, la isoleucina y la alloisoleucina, y la interferencia isobárica hidroxiprolina, significa que un resultado elevado de "leucinas" no siempre equivale al diagnóstico de la enfermedad de la orina de jarabe de arce (una enfermedad metabólica hereditaria que es la única causa conocida de una alloisoleucina elevada). La prueba ideal de segundo nivel en este escenario es una técnica basada en la separación que resuelve y cuantifica todas las especies isobáricas de leucina de la muestra de la mancha de sangre. Si la aloisoleucina es indetectable y las concentraciones de otros aminoácidos de cadena ramificada no son notables en la prueba de segundo nivel, es posible descartar el riesgo de MSUD, y no es necesario hacer un seguimiento con análisis de aminoácidos plasmáticos y ácidos orgánicos en orina.
Un ejemplo de un resultado de prueba con un bajo valor predictivo positivo debido a una baja especificidad diagnóstica es el hallazgo de una propionilcarnitina elevada en la prueba de cribado primario de las acidemias propiónica o metilmalónica. El aumento de la propionilcarnitina también puede encontrarse en bebés nacidos de madres con una deficiencia grave de vitamina B12. Cuando se detecta un aumento de la proprionilcarnitina mediante el cribado de manchas de sangre secas, la adición de una medición de segundo nivel de los ácidos orgánicos en la mancha de sangre mediante LC-MS/MS3 puede revelar rápidamente si el patrón de metabolitos sugiere una enfermedad en el recién nacido (y en este caso, cuál de los dos trastornos es más probable), o bien, una deficiencia vitamínica materna. Históricamente, la investigación de una mancha de sangre elevada de propionilcarnitina desencadenaba una secuencia de eventos de seguimiento que implicaban volver a llamar al bebé para realizar más pruebas, lo que es comprensiblemente angustioso para la familia, y un drenaje de recursos para el proveedor de servicios.
Un ejemplo de una prueba en la que tanto la especificidad analítica como la diagnóstica contribuyen a una elevada tasa de falsos positivos son las mediciones por inmunoensayo basado en fluorescencia de la mancha de sangre seca de 17-hidroxiprogesterona (17-OHP) en el cribado de la hiperplasia suprarrenal congénita (HSC). La prematuridad, el bajo peso al nacer y el sufrimiento neonatal se asocian a una elevación transitoria de la 17-OHP, así como a una serie de otras hormonas esteroides estructuralmente relacionadas, algunas de las cuales pueden presentar reacciones cruzadas con los anticuerpos del inmunoensayo. Realizar el análisis de los esteroides suprarrenales por LC-MS/MS permite distinguir la 17-OHP de otras hormonas no asociadas a la HAC. También permite la cuantificación multiplexada de cortisol, androstenediona, y 11- y 21-deoxicortisol, que, cuando se combinan en un cálculo de ratio, pueden predecir con un mayor grado de certeza si la elevación de 17-OHP está realmente asociada a la HAC, o, si está presente alguna otra condición benigna, que no necesita seguimiento.
Un análisis retrospectivo de cuatro años de datos de cribado de la Clínica Mayo de Minnesota demostró que la introducción de una prueba de segundo nivel para detectar esteroides suprarrenales tras un cribado primario de 17-OHP basado en un inmunoensayo sólo produjo 211 derivaciones, con un coste total de algo más de 270.000 dólares tanto para la clínica como para el laboratorio. Si no hubiera existido la prueba de segundo nivel, hasta 2712 casos habrían necesitado seguimiento, con un coste estimado de 2,3 millones de dólares. La introducción de la prueba de segundo nivel basada en LC-MS/MS significó que la cantidad de dinero gastada en la investigación de los bebés no afectados se redujo de 8 dólares por nacimiento vivo a sólo 80 céntimos. Dado que el coste del cribado de los recién nacidos en Minnesota se estima actualmente en 101 dólares por caso,5 esto representa un enorme ahorro de eficiencia. Un ahorro que podría reinvertirse para la futura expansión del cribado.
Recursos:
-
- Diez grandes logros en materia de salud pública - Estados Unidos, 2001 - 2010.
- Schmidt, J.L. et al. The impact of false-positive newborn screening results on families: a qualitative study. doi: 10.1038/gim.2011.5.Genet Med. Jan;14(1):76-80. 2012.
- Monostori, P. et al. Determinación simultánea de ácido 3-hidroxipropiónico, ácido metilmalónico y ácido metilcítrico en manchas de sangre seca: Ensayo LC-MS/MS de segundo nivel para el cribado neonatal de la acidemia propiónica, las acidemias metilmalónicas y los trastornos combinados de remetilación. PLoS ONE. Sept;12(9). https://doi.org/10.1371/journal.pone.0184897.2017.
- Matern, D. et al. Reducción de la tasa de falsos positivos en el cribado neonatal mediante la implementación de pruebas de segundo nivel basadas en MS/MS: La experiencia de la Clínica Mayo. JIMD. Aug;30(4):585-592. 2007.
- Centro Nacional de Cribado del Recién Nacido y de Recursos Globales: https://genes-r-us.uthscsa.edu/resources/consumer/statemap.htm. 3 de noviembre de 2014.
Más información sobre el cribado neonatal basado en la espectrometría de masas:
Temas populares
ACQUITY QDa (16) bioanálisis (11) biológicos (14) biofarmacia (26) biofarmacéutica (36 ) biosimilares (11) bioterapéutica (16) estudio de caso (16) cromatografía (14) integridad de los datos (21) análisis de alimentos (12) HPLC (15) LC-MS (21 ) cromatografía líquida (LC) (19) detección de masas (15) espectrometría de masas (EM) (54 ) desarrollo de métodos (13) STEM (12)