¿Retener o no retener? ¿Cuánto es suficiente retención?

En los diversos trabajos colaterales que hemos publicado en Waters sobre plaguicidas altamente polares, como el glifosato o el clormecuat, uno de los principales parámetros que discutimos es la retención. Pero, ¿qué queremos decir con la palabra retención?
- El tiempo de retención (TR) es el tiempo que transcurre entre el inicio de una inyección y la aparición del pico máximo del analito oanalitos1.
Sin embargo, necesitamos saber cuánta interacción tiene el analito con el material de la fase estacionaria (el tiempo relativo que interactúa con la fase estacionaria frente a la fase móvil).
- El factor de retención (k), que antes se denominaba factor de capacidad, es la medida del tiempo que el analito o analitos objetivo residen en la fase estacionaria en relación con el tiempo que residen en la fase móvil1.
Si esta interacción es demasiado corta, entonces no se ha producido ninguna o poca cromatografía, las separaciones serán menos estables y habrá una alta probabilidad de supresión de iones cuando se utilice la LC-MS.
- El volumen vacío de la columna (v) es una medida del volumen interno dentro de la columna empaquetada con las partículas de la fase estacionaria y puede estimarse a partir de la longitud de la columna (L) y el diámetro interno (ID).
- Volumen vacío de la columna (µl) = 0,66 x π x (diámetro interno de la columna/2)2 x L
Para la mayoría de las columnas Waters empaquetadas con partículas totalmente porosas puede utilizarse un valor de "volumen de poros" de 0,66. Las partículas superficialmente porosas(por ejemplo, el núcleo sólido), tienen menos volumen, por lo que se suele utilizar un valor de 0,49.
por ejemplo, para una columna ACQUITY HSS T3 de 3,0 mm x 100 mm, v = 0,467 mL
Conociendo el volumen de vacío de la columna y el caudal utilizado se puede calcular el tiempo de vacío de la columna (t0):
t0 = V/F
Una respuesta más precisa se encontrará midiendo el volumen vacío de su columna cuando esté instalada en el sistema de LC, inyectando un compuesto que usted sabe que no está retenido.
Lo anterior es un ejemplo de la retención de un pesticida relativamente polar, el metamidofos, utilizando las condiciones típicas de la cromatografía líquida (CL) de fase inversa de residuos múltiples.
Las directrices de control de calidad analítica, rendimiento y validación de métodos, como SANTE/12682/20192 y la Decisión 2002/657/CE de la Comisión3 , establecen que "el tiempo de retención mínimo aceptable para el analito o los analitos debe ser al menos el doble del tiempo de retención correspondiente al volumen vacío de la columna".
En el ejemplo anterior se puede ver que la columna y las condiciones de LC utilizadas proporcionan una retención suficiente del metamidofos, de acuerdo con las directrices de SANTE.
Si también nos fijamos en el factor de retención (k), la medida de la retención de una columna en relación con el tiempo de vacío de la columna (t0):
k = (tR - t0)/ t0
Asegúrese de que el pico de elución más temprano tenga un valor de k >1,0 y preferiblemente >1,5.
Cuando uno se enfrenta a analitos aún más polares, como los pesticidas iónicos polares, se aplican las mismas reglas, independientemente de la elección del sistema cromatográfico. Es muy poco probable que se consiga una retención suficiente para estos compuestos utilizando los típicos flujos de trabajo en fase inversa.
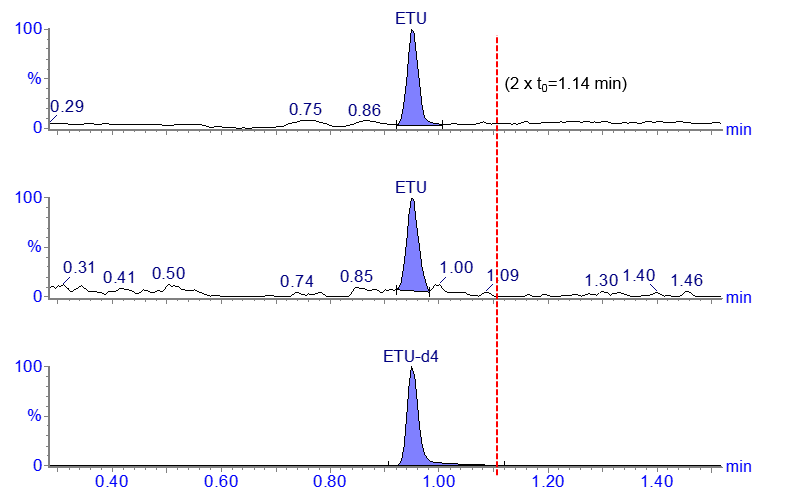
El cromatograma siguiente muestra el análisis LC-MS/MS de un compuesto altamente polar, la etilenotiourea (ETU).
Este es un desarrollo de método temprano, cromatograma de ejemplo de una columna HILIC (2,1 x 50 mm, 1,7 µm) utilizando un flujo de 0,2 mL/min.
- El volumen vacío de esta columna de 2,1 x 50 mm es de 0,114 mL
- El caudal es de 0,2 mL/min, por lo que t0 es de 0,57 minutos (2 x t0=1 ,14 min)
El tiempo de retención de la ETU en este caso es inferior al doble del tiempo de vacío de la columna (t0) con las condiciones de la fase móvil que se han utilizado.
Las opciones para la retención y separación de analitos altamente polares pueden incluir la cromatografía iónica, las columnas de carbón grafitado/grafítico poroso y la cromatografía HILIC/de modo mixto. El siguiente cromatograma muestra la retención de varios plaguicidas polares aniónicos utilizando la columna Anionic Polar Pesticide (APP) de Waters.
La fase estacionaria de la columna consiste en partículas híbridas con puente de etileno (BEH) con ligandos de dietilamina (DEA) con enlace trifuncional. La combinación de la superficie hidrofílica y las propiedades de intercambio aniónico de los ligandos proporciona características cromatográficas muy adecuadas para la retención y separación de compuestos aniónicos altamente polares.
En estas condiciones4, utilizando una columna de APP de 2,1 mm x 100 mm con un caudal de 0,5 mL/min, el t0 es de 0,46 minutos, por lo que el RT para el AMPA, el primer pico en eluir, es de 3,5 x t0, muy dentro de las directrices de SANTE.
Por lo tanto, si desarrolla un método de LC desde cero o implementa un método existente tomado de otro lugar, no se centre únicamente en el valor del tiempo de retención, sino que intente asegurarse de que el tiempo de retención para el analito sea al menos el doble del tiempo de retención correspondiente al volumen vacío de la columna, en las condiciones utilizadas.
- Appendix: HPLC Nomenclature, Waters Corporation: https://legacy-stage.waters.com/waters/en_US/Appendix%3A-HPLC-Nomenclature/nav.htm?cid=10049080&locale=en_US
- Documento nº SANTE/12682/2019. Procedimientos de control de calidad analítica y validación de métodos para el análisis de residuos de plaguicidas en alimentos y piensos.
- 2002/657/CE: Decisión de la Comisión, de 12 de agosto de 2002, por la que se aplica la Directiva 96/23/CE del Consejo en cuanto al funcionamiento de los métodos analíticos y la interpretación de los resultados y Contaminantes 22(3): 245–250. http://dx.doi.org/10.1080/02652030500110618
- Determinación de plaguicidas polares aniónicos en productos alimenticios con alto contenido de agua, Waters Technology Brief 720006645 (2020)
Temas populares
ACQUITY QDa (16) bioanálisis (11) biológicos (14) biofarmacia (26) biofarmacéutica (36 ) biosimilares (11) bioterapéutica (16) estudio de caso (16) cromatografía (14) integridad de los datos (21) análisis de alimentos (12) HPLC (15) LC-MS (21 ) cromatografía líquida (LC) (19) detección de masas (15) espectrometría de masas (EM) (54 ) desarrollo de métodos (13) STEM (12)