Capítulo y verso: La USP 621 y usted

In August 2014, the United States Pharmacopeia and the National Formulary (USP-NF) put into effect new guidelines to “allowable adjustments” in its Chapter <621> (USP37-NF32 S1). And as of August 1, 2016 when USP 39 NF 34 S1 goes into effect, for <621> nothing significant has changed since.
La USP no hace públicos los cambios en sus directrices de manera evidente, pero estos cambios se anunciaron en su sitio web mucho antes de que entraran en vigor las nuevas directrices.
No son reglamentos, en sí mismos. Pero, al menos en EE.UU., la Administración de Alimentos y Medicamentos (FDA) los trata como parámetros para sus reglamentos.
Así que, al igual que un peatón que camina por las vías en la trayectoria de un tren que se aproxima, probablemente sea mejor prestar atención a las luces intermitentes, para no encontrarse en el extremo equivocado de 10.000 toneladas de acero que se mueven rápidamente.
(Alerta de spoiler: el tren siempre gana).
USP Chapter <621>, you say?
The USP-NF is a book of pharmacopeial standards that has been designated by the FDA as the official compendia for drugs marketed in the United States. Its chapter on Chromatography is <621>, found here, and “defines the terms and procedures used in chromatography and provides general information.” Specifically, it explains the allowable adjustments to chromatography systems in order to meet system suitability requirements.
Una guía de directrices.
Los cambios recientes han sido influenciados por un documento de estímulo de 2009 escrito por el Dr. Uwe Neue et al, que proponía aplicaciones de base científica de los métodos de gradiente. Aunque este documento sugería cambios en la transferencia de métodos tanto isocráticos como de gradiente, el USP ha implementado los cambios sólo en los métodos isocráticos.
Anteriormente, se permitían los cambios relativos al tamaño de las partículas, suponiendo que los cambios se reducían al 50%. La longitud de las columnas podía aumentarse o reducirse en un 70%, los caudales podían aumentarse o reducirse en un 50% y el diámetro interior de la columna podía cambiar a voluntad. ¿Flexible? Sí. Bueno, aparentemente - pero, una reducción del 50% en un tamaño de partícula de 5 µm sólo nos lleva a 2,5 µm, no a las más recientes partículas de menos de 2 µm.
Ahora, para los métodos isocráticos, los cambios en el tamaño de las partículas y la longitud de la columna se tratan como una relación, en lugar de parámetros discretos, que pueden disminuir un 25% o aumentar un 50%, mientras que el caudal puede seguir aumentando o disminuyendo un 50%. Cualquier cambio realizado en el diámetro interior de la columna está permitido. Dependiendo de la longitud de su columna, las partículas más nuevas de menos de 2 µm pueden estar ahora disponibles para su uso, sin necesidad de validación.
Sin embargo, para los métodos de gradiente, no se permiten cambios en ninguno de los siguientes aspectos: tamaño de las partículas, longitud de la columna, caudal o diámetro interior de la columna.
¿Sigues conmigo?
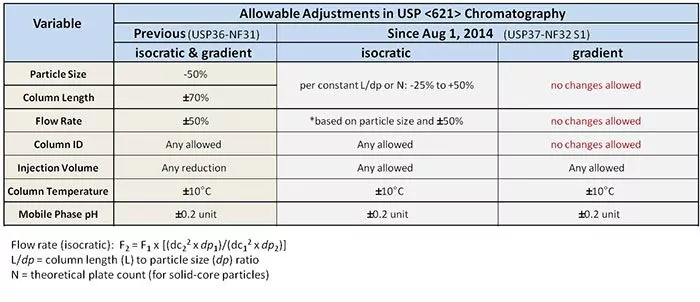
Vea la práctica tabla de abajo. Porque, fotos.
Gracias por la foto, ¿ahora qué significa todo esto?
Al mantenerse dentro de los parámetros de los "ajustes permitidos" de los métodos isocráticos, los analistas pueden realizar simplemente la verificación del rendimiento del método y evitar los pasos de revalidación que requieren mucho tiempo.
Y así...
Así pues, los cromatógrafos tienen ahora una mayor capacidad para aplicar la tecnología de columnas más novedosa sin dejar de respetar las monografías existentes. Esto significa, en resumen, la oportunidad de adoptar métodos más avanzados en el laboratorio que, al final, pueden conducir a la reducción del consumo de disolventes, tiempos de análisis más rápidos y un aumento general del retorno de la inversión.
No, no se encontrará con una muerte inminente si no adopta la UPLC/UHPLC.
Al menos, todavía no. Para los que utilizan métodos isocráticos, el camino hacia una plataforma UPLC está bien iluminado. Según un libro blanco publicado por Waters, "la flexibilidad de las nuevas directrices abre ahora la posibilidad de transferir los métodos isocráticos anteriores de HPLC a UPLC sin la inversión de tiempo y las molestias de la revalidación, al tiempo que se obtiene la eficiencia general del laboratorio y las ganancias de productividad de los ensayos de mayor rendimiento".
Dicho de forma más sencilla, el aprovechamiento de la tecnología de columnas de partículas de menos de 2 µm puede suponer un ahorro de tiempo de casi 10 veces y una reducción del consumo de disolventes de más de 15 veces. Añada a esto herramientas como el Gestor de Validación de Métodos (MVM) de Empower 3, que le permite realizar la validación de métodos cromatográficos -desde la planificación del protocolo hasta el informe final- en una sola aplicación, y reduzca el tiempo y el coste de la validación de métodos hasta en un 80%.
Te dejaré hacer las cuentas. O ahórrate el tiempo y deja que Waters haga las cuentas por ti.
Por desgracia, los métodos de gradiente son más populares en su uso.
Sin embargo, dadas las nuevas directrices, cualquier cambio en la configuración de las columnas de los métodos existentes requiere ahora una revalidación completa.
¿Cuándo un método no cumple los requisitos de idoneidad del sistema? Revalidación.
¿Actualmente utiliza un método de compendio con modificaciones que antes estaban permitidas? Ya no lo están.
Al menos, no sin revalidar.
Ahora, esto no es una razón para ir todo el espacio de la oficina en su sistema de HPLC y luego correr a comprar una plataforma UPLC. (Si por alguna razón decides seguir este camino, asegúrate de grabarlo en vídeo. Ya sabes, "viral").
Pero, aunque la HPLC sigue teniendo una excelente robustez, y usted puede seguir ejecutando los métodos heredados sin tener que hacer ningún cambio importante en su tecnología, podría valer la pena considerar la revalidación en las mejores herramientas disponibles. Hacerlo con una tecnología antigua podría suponer una pérdida de tiempo y recursos.
Diversión con los acrónimos: CQA y QbD.
Al concebir la UPLC hace una década, Waters permitió a sus clientes no sólo ir más rápido, sino también ver más.
Ver más significa ser capaz de reconocer mejor los Atributos Críticos de Calidad (CQA), para que los analistas puedan entender mejor los productos. Tener acceso a una mejor información significa tener la capacidad de tomar mejores decisiones.
Todo ello está relacionado con un enfoque de calidad por diseño (QbD) de un producto, en el que la calidad se incorpora tanto al producto como al proceso, mitigando el riesgo en la fabricación y el análisis del producto.
Y ahora, después de la lección sobre la sopa de letras, ¿qué tiene que ver esto contigo?
Francamente, el tren de acero mencionado anteriormente. Además, por no hablar de sus clientes.
La FDA ha publicado una guía para que los analistas empiecen a pensar más en el ciclo de vida de sus métodos. Por ejemplo, si un método sigue sin cumplir los requisitos de idoneidad del sistema, quizá sea el momento de pasar a una tecnología más nueva, como la UHPLC o la UPLC, para conocer mejor ese método.
En resumen, entienda lo que hay en la salsa, y deje de limitarse a seguir el libro de cocina.
Los consumidores también se benefician, en última instancia, de que los laboratorios se pasen a la nueva tecnología de alta resolución y puedan saber más sobre un producto. En la última década se han dado a conocer varios casos en los que se ha utilizado la tecnología UPLC para descubrir peligros hasta entonces desconocidos en los productos, como la melamina en los preparados para lactantes y las complicaciones/muertes relacionadas con la heparina.
La ciencia no deja de avanzar.
Y con ello, tampoco la normativa. Este paso de la USP hacia la modernización de los métodos introduce un oportuno punto de consideración con respecto al uso del tiempo y de los valiosos recursos de los laboratorios y, en última instancia, de las empresas preocupadas por sus ciclos de vida de la tecnología y el correspondiente rendimiento de las inversiones tecnológicas.
Recursos adicionales:
- Future-Proof Solutions for Regulated Laboratories In the Face of Changing USP <621> Guidelines
- Volumen de permanencia y volumen extracolumna: Qué son y cómo influyen en la transferencia del método
- Modernización del método USP mediante cambios permitidos de "L/dp equivalente" y "N equivalente" con columnas CORTECS C8 de núcleo sólido
Temas populares
ACQUITY QDa (16) bioanálisis (11) biológicos (14) biofarmacia (26) biofarmacéutica (36 ) biosimilares (11) bioterapéutica (16) estudio de caso (16) cromatografía (14) integridad de los datos (21) análisis de alimentos (12) HPLC (15) LC-MS (21 ) cromatografía líquida (LC) (19) detección de masas (15) espectrometría de masas (EM) (54 ) desarrollo de métodos (13) STEM (12)